|
洁净技术是一门多学科的综合性较强的技术领域。
洁净室要求提供一个受控尘埃粒子污染的空气洁净度达到规定级别的可供人活动的空间。其功能是控制微粒的污染。为了达到规定的洁净度级别,有效地控制微粒的污染,使人们在其中从事精密的生产和科学实验活动。
洁净室绝不是仅限于“洁净”,而必须是一个对冷热、噪声、照度、静电、微振都有相当要求的多功能的综合体
洁净厂房的主要组成如下图:
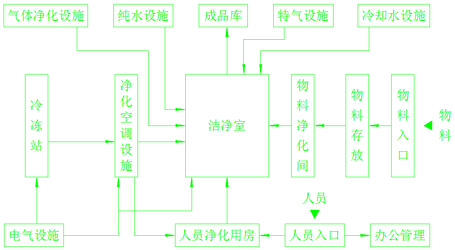
(点击放大)
成功的洁净厂房首先要有很好的建筑平面布置和空间布置,要考虑人流、物流的动线,要根据机电管线的路由设置必要的技术夹层和技术夹道。要考虑生产发展的灵活性。还要注意洁净厂房的防火和疏散。
一、洁净室围护结构
选择洁净室围护结构的装饰材料的关键:要保证洁净室的气密性和材料表面不发尘、不滞留微粒、不积尘。还要注意装修和人体产生的静电效应。
装配式洁净室的吊顶和隔墙一般采用金属壁板(彩钢岩棉夹芯板、彩钢石膏夹芯板、彩钢酚醛夹芯板等)
洁净室的地面一般采用水磨石地面、环氧树脂自流平型地坪、聚氨酯涂料、防静电PVC塑料地板或防静电高架通风地板。
(金属壁板及地面的照片)
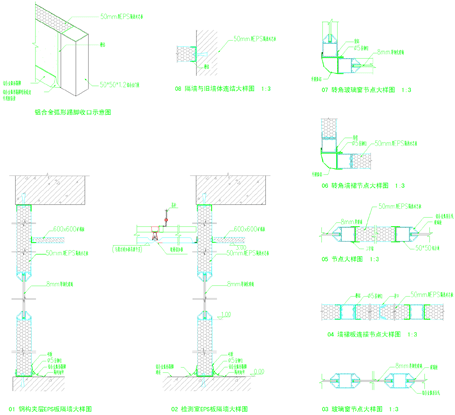
(点击放大)
二、洁净室空气净化――要求至少经过粗、中、高效三级过滤
1.集中式净化空调系统
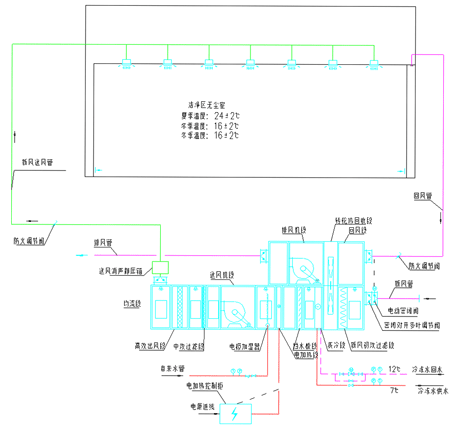
(点击放大)
2.分散式净化空调系统
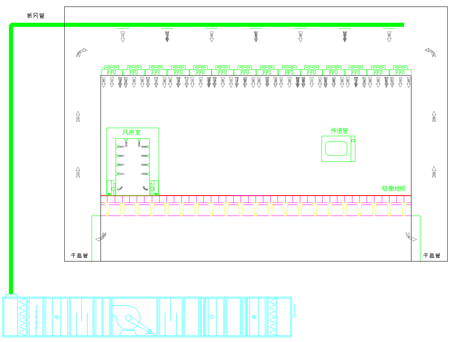
(点击放大)
按气流流型分类:
单向流洁净室――气流方式的基本形式类似气缸内的活塞运动,将污染源散发出的尘、菌污染物在尚未向室内扩散之前就被压出室外;洁净空气对污染源起到隔离作用,隔断尘、菌污染物向室内扩散。
非单向流洁净室――以稀释方法达到净化目的,用经过高效过滤器处理的洁净空气将污染物冲淡稀释,从而保持室内所需的空气洁净度等级。
混合流及其洁净室――混合流洁净室是将非单向流流型和单向流流型在同一洁净室内组合使用。单向流洁净室的设备费和运行费都很高,但在某些实际洁净室工程中往往只是部分区域有严格的洁净度要求,而不是整个洁净室(区)。混合流洁净室的特点是在需要空气洁净度严格的部位采用单向流流型,其他则为非单向流流型。这样既满足了使用要求,也节省了设备投资和运行费用。混合流洁净室的一般形式为整个洁净室为非单向流洁净室,在需要空气洁净度严格的区域上方采用单向流流型的洁净措施,使该区域得到满足要求的单向流流型洁净区,以防止周围相对较差的空气环境影响局部的高洁净度。
3.洁净室相关设备及部件(图片见《产品展示》)
洁净工作台
层流罩
余压阀
传递窗
风淋室
货淋室
三、洁净厂房的动力设施
1.冷冻站房
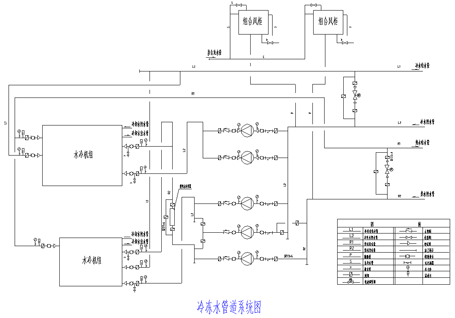
(点击放大)
2.纯水制备系统 (点击进入是否可用“奥星”图片进一步说明)
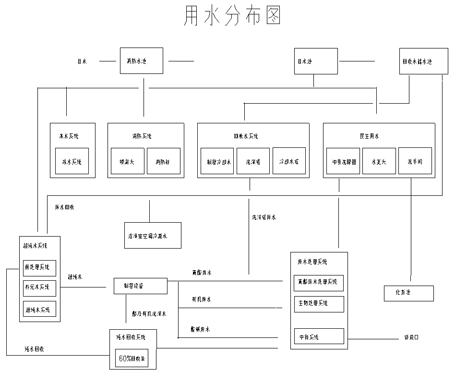
(点击放大)
3.压缩空气、真空、氮气管道系统图
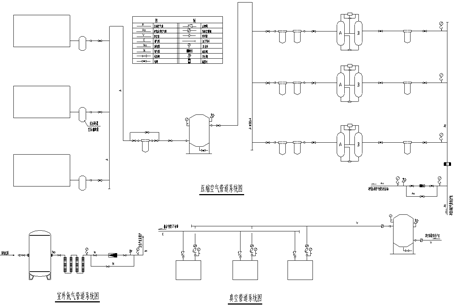
(点击放大)
4.电气设备与照明
四、洁净室涉及其它技术领域――环境控制
1.微振动控制
2.静电防护
3.电磁干扰的防止
4.噪声控制
GMP――药品生产质量管理规范(Good Manufacturing Practice)
药品实施GMP制度是国家对药品生产企业监督检查的一种手段,是药品监督管理的重要内容,也是保证药品质量的一种科学的先进的管理方法。
国家药品监督管理局负责全国药品GMP认证
国家药品监督管理局药品认证管理中心承办药品GMP认证的具体工作
EU GMP――欧盟 GMP 指南
FDA――美国食品药品管理局
EU GMP认证
生物洁净室――以有生命微粒的控制为对象
应用行业:制药、生物工程、医疗卫生、食品、化妆品、动物实验室、生物学安全实验室等
GMP认证是集软件、硬件、安全、卫生、环保于一身的强制性安全认证。
国际认证的意义本身就是不仅要加强药厂内部诸多质量因素的过程控制,也要对药厂外部关键质量因素有所控制。
洁净室技术是实施GMP的一个必要条件:
药品生产环境控制的目的是为了防止因污染或交叉污染等危及产品质量的情况发生。
药品生产用洁净室的污染控制对象包括尘粒和微生物,空气中的微生物主要附着在尘粒上。
制药工业净化空调的最大特点是,制造工序本身就是粉尘发生源,特别是固体制剂的制造工序更为突出。在这一类洁净室内,采用局部除尘方式效果最好,而且也很经济。如果发尘量较多的操作室没有采用局部除尘装置,而只靠空调方式要达到100000级的洁净室,其空调费用很可能超过无菌室的造价。但是,由于微小的粉尘很容易飞扬,例如100um以下的粒子,在0.5m/s的微风下也能扬起,无疑吸尘过强会增加药品损耗。
在注射类无菌制剂的生产中,如果对药品不做高压蒸汽消毒等最后的灭菌处理,而只是在无菌条件下把无菌原料加以配制和灌封的方法进行生产,那么这样的无菌操作室一般按落下细菌数为1以下(直径为9cm的器皿上,在一小时内)的生物洁净室加以管理
最后作灭菌处理的一般注射剂的配制和灌封室或者在无菌状态下生产其他制剂的操作室也作为无菌净化区域加以管理。随着GMP的贯彻,有一些非无菌制剂的生产过程中,把交叉污染和微生物污染也作为一个问题处理
空气净化设备是对生产设备和生产管理的完善和补充。防止微生物污染或交叉污染只依靠空气调节是不行的,即使有了净化设备也不一定能完全满足GMP要求,必须注意,当设备条件达到一定水平后,还要通过管理加以实现。
青霉素容易飞扬和悬浮,其空调系统要和非青霉素制剂的操作室分开,单独设置,防止交叉污染,并且与其他操作室空调系统新风口之间保持一定距离。单独设置空调系统的目的在于,使排风构成直流系统,防止青霉素类抗生素操作室的空调调再循环到其他制剂的操作室。
一般来说,生产固体制剂时,在称量、混合、制粒、干燥、制片、密封填充、粉末填充等各工序中,粉体都在干燥状态下进行处理。不可避免地会产生药尘。因而除了操作室的平面布置或结构以及产生粉尘的部位采用局部排风等措施外,还要通过层流等空调方式,综合解决交叉污染问题。
青霉素等特殊制剂的制造中,内部粉尘不允许流向外部。在这种情况下,必须单独设置操作室或者把做成负压,使压力低于其它操作室。特别是操作室的围护结构体直接与大气接触时,一定要严加密封
药品GMP认证管理办法:
第五条 申请药品GMP认证的药品生产企业(车间),应按规定填报《药品GMP认证申请书》一式二份,并报送以下资料
1、《药品生产企业许可证》和《营业执照》(复印件);
2、药品生产管理和质量管理自查情况(包括企业概况、GMP实施情况及培训情况);
3、药品生产企业(车间)的负责人、检验人员文化程度登记表;高、中、初技术人员的比例情况表;
4、药品生产企业(车间)生产的组织机构图(包括各组织部门的功能及相互关系,部门负责人);
5、药品生产企业(车间)生产的所有剂型和品种表;
6、药品生产企业(车间)的环境条件、仓储及总平面布置图;
7、药品生产车间概况及工艺布局平面图(包括更衣室、盥洗间、人流和物料通道、气闸等,并标明空气洁净度等级);
8、生产剂型或品种工艺流程图,并注明主要过程控制点;
9、药品生产企业 (车间) 的关键工序,主要设备验证情况和检验仪器、仪表校验情况;
10、药品生产企业 (车间) 生产管理、质量管理文件目录。
工业洁净室――以无生命微粒的控制为对象
应用行业:精密工业、电子工业、宇航工业、化学工业、原子能工业、印刷工业、照相工业
彩管产业、微电子产业、光电子、光机电一体化产业等
工业洁净室对洁净生产环境提出更新、更高的要求:
1.工业洁净室对空气净化的控制范围已从尘粒发展到分子污染、化学污染――采用去除分子态污染物、化学污染物的活性炭过滤器、泰氟隆(PTFE)空气过滤器、化学过滤器等,并配套相应的检测手段。
2.工业洁净室要控制生产加工过程中的清洗用水、蚀刻用化学品、反应气体和运载气体等的杂质含量――A.采用超高纯材料。要求提供对纯度、杂质含量的要求非常严格的超纯气体、超纯水等。B.由于较多地使用毒性气体和溶剂,室内必须设置局部排风设备。为保持室内正压,新风量要比排风量大。C.生产工艺中的原料既有酸类,又有溶剂类,针对不同的情况,室内装修面层前者采用聚乙烯类材料,后者要采用不锈钢材。
3.工业洁净室的温度、相对湿度、防静电、防微震、噪声、照度等要求控制在非常严格的范围内。――A.室内温湿度变化应限制到最小 ,以防止产品膨胀或收缩。为了对亚微米、深亚微米级的集成电路的图形加工,必须把暴光设备的环境温度的变化控制在+0.1C以下,光刻胶的溶胶工序的生产环境的相对湿度变化控制在2%~5%以下。B.各种光刻设备、尺寸测量仪器的安装基础应充分考虑防微震问题。C.照相制版工序中,根据感光材料性能的要求,其照明以及门窗玻璃和出入口等应考虑遮光措施。一般的作业要求600lx以上的照度。
4.空调设备通常24小时连续运转,应考虑发生故障时的补救措施。室内的气体、水和电气等管线的布置要考虑改建方便。
|

